新年起首,Deepseek的横空出世搅拌了全产业创新的风浪,数据资源的高效欺骗,进一步成为了新一轮科技鼎新的关节之战,也成为了本年“两会”上各方要点情怀的提议,在《政府使命敷陈》中也明确,“加速完善数据基础轨制,深切数据资源开发利用,促进和范例数据跨境流动”。
我国精深的患者数目使咱们领有世界上潜在范围最大的医学数据资源,将这些资源升沉为创新资源将极地面助力我国生物医药产业发展。当今,我国医学大数据在维度、广度和深度都在快速增长。各大医学机构已拓荒了完备的电子信息采集、记载、处理和分析系统,包括临床医学相干数据、生物信息数据、病院信息系统数据、医疗卫生职业平台数据、大家卫生普查数据等,将临床全经由数字化这些临床数据不仅提高了诊疗的遵守和精确度,更是精确医学的主要基础,为填补临床空缺、幽闲患者需求的创新药研发提供了多数谨慎的资源。
但是,尽管各大医疗机构存在多数数据资源存量,却未升沉为资源增量。字据现存相干遵守[①][②],集合中国药促会调研发现,当今各病院数据处分溜达,不同病院以至不同科室、不同课题组之间临床信息系统各成孤岛,数据体式和范例不一、数据交织机制劳作,部分数据以至还存在合规处分不严格、苦衷保护机制不完善、数据质地不高级问题。当新药研发团队思要取得临床数据资源助力临床相干时,发现难以全面取得,也短缺畅通的数据来往渠谈,即使在部分已完成的来往中,也出现了产权确权弯曲、估价订价范例不一、信任机制不完善等问题[③]。
何如买通刻下临床数据分享和来往的堵点?本文将从外洋训戒先容开赴,共同考虑临床数据分享与来往机制的拓荒所在。
一
目
外洋训戒:临床数据资源驱动医药创新的关节智商
1
顶层遐想:构建数据分享和来往的法律基础
将临床数据有关骨子写入法律,是保障数据安全、明确权属和领域、开释数据价值的基础,是数据分享和来往机制得以运行的弥留复旧。
好意思国于2012年发布的《21世纪养息法案》(21st Century Cures Act),异常提到了要通过临床数据的分享促进科学跨越和大家卫生,饱读吹政府、科研机构、临床相干机构、药企和患者组织之间通过数据分享公约明确各方的职权和义务,这些公约经常包括数据的使用范围、使用期限、数据安全要求以及利益分派机制等骨子。但同期也明确数据合规性要求,关于个东谈主健康信息等数据,必须严格遵命1996年颁布的《健康保障可携性和职遵法案》(HIPAA),这不仅保护了患者的苦衷权,还为数据的正当来往和确权提供了法律依据。
2013年5月,好意思国政府发布《绽开数据战略-将信息动作钞票进行处分》(0pen Data Policy-Man-aging Infommalion as an Asset)备忘录,要求各机构以支捏下贱信息处理和传播行径的花样汇集或创建电子数据信息,包括使用绽开体式、数据范例等,最大甩手地提高数据的互操作性和信息可造访性。
跟着顶层遐想的明确,NIH立时发布了一系列临床数据分享的具体落实战略,对临床相干的数据建议了必须大约已毕分享的硬性要求:
表1 NIH数据钞票处分与分享战略[④]
欧盟则通过《通用数据保护条例》(GDPR)为医学数据的分享和来往提供了法律保障。GDPR不仅规定了数据的苦衷保护要求,还明确了数据主体的职权,如数据造访权、数据删除权等。同期,欧盟还通过《欧洲健康数据空间》(EHDS)运筹帷幄,推动成员国之间的健康数据分享,为数字医疗职业和家具培植单一阛阓。
此外,英国、加拿大等国度也接踵出台了有关法律规定,如英国的《数据保护法案》《数据战略通用原则》《数据处分和分享战略》;加拿大的《基因组数据发布与分享战略》《个东谈主信息保护与电子文献法》(PIPEDA)等,都对临床机构和团队明确建议了数据质地和分享的要求,明晰数据处均权责,也为临床数据的分享和来往提供了依据,促进了医学大数据的流通和价值挖掘。
2
调处范例:确保数据互操作性和质地
调处范例的制定和履行不仅提高了数据的互操作性,还普及了数据的质地和可靠性。临床数据源文献溜达在诊疗、随访、临床锤真金不怕火等不同的业务系统中,结构、采集花样的不同导致呈现效果各异,对不同来源的临床数据进行范例化是一个精深的工程。通过接受调处的数据体式、编码体系和元数据范例,医学大数据的分享来往变得愈加高效和准确,为数据分析和应用提供了坚实的基础。
举例,在临床锤真金不怕火数据范例化方面,为提高临床数据质地,促进外洋相助和疏导分享,多个外洋组织开发了各项数据范例,成功和隆起的是CDISC系列范例,它与用于病院医疗系统信息与临床锤真金不怕火数据交换的HL7、外洋范例化组织(IOS)范例、用于实验室信息语义范例化的LONIC及ICH开发的医学范例术语MedDRA等也有兼容和一致性。
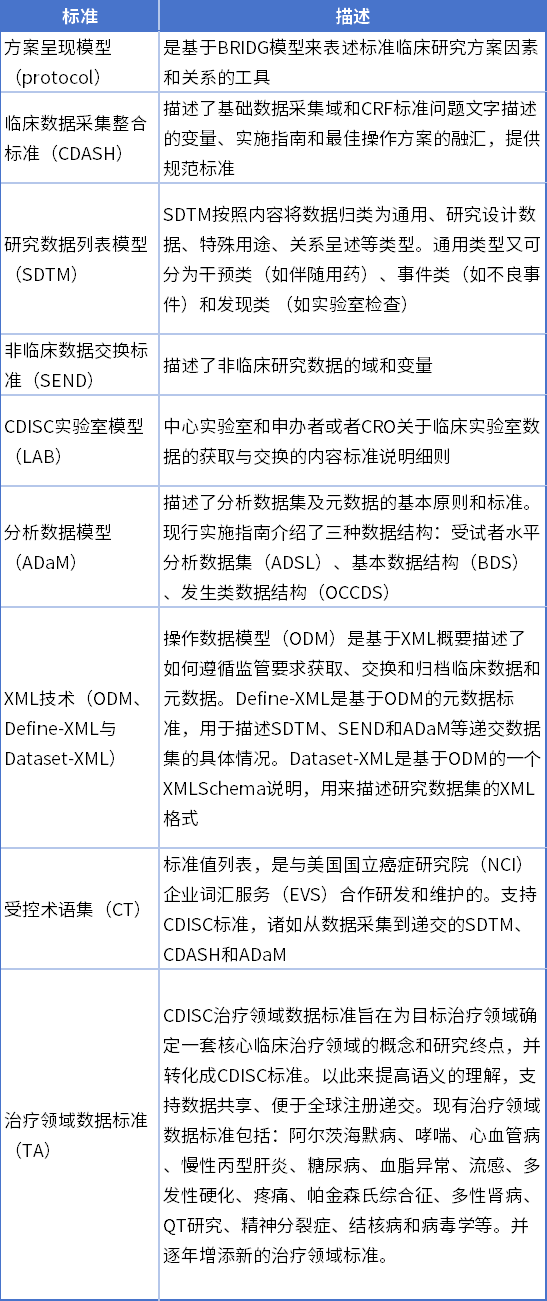
表2 CDISC中枢范例一览表[⑤]
FDA自2014年已发布文献强制要求电子提交的花样需苦守CDISC范例,随后日本PMDA、欧洲的EMA也明确建议使用CDISC范例的要求并发布肃肃文献加入强制要求。在多国监管部门的勤恳下,CDISC数据范例的使用在外洋范围扩大化,一些业内主流数据处分软件、数据分析软件等也开发、镶嵌了CDISC范例化数据模块,加多了范例的通用性和可及性。当今我国多家创新药企业也加速关于CDISC的引入,加速外洋临床锤真金不怕火的开展和外欧化程度。
跟着东谈主工智能(AI)工夫的赶紧发展,何如借助AI的苍劲功能促进临床信息系统的拓荒处分并推动数据范例化拓荒,已成为临床数据资源挖掘的新所在[⑥]。
3
统筹集聚:构建数据分享和来往的平台
在法律对医学数据的分享和来往明确的基础上,还需要依托于苍劲的集聚基础设施。外洋上,很多国度和地区通过设立临床相干集聚,汇集世界高质地临床数据和患者资源信息,设立临床数据库和病东谈主样本资源库已毕了数据的聚积处分、分享,并鼓励公私相助和来往,提高世界临床相干和新药研发的效果和遵守。
表3 列国大型临床数据和分享平台
二
目
发展所在和建议
刻下,我国已具备临床数据资源储存、分析与处分的硬件设施资源和工夫条目,部分地区已启动入辖下手医疗数据使用和赋能生物医药产业发展的尝试[⑦]。但是规定战略的完善、与外洋接轨的数据范例化、数据扫数权和使用权的明确、合规来往空间的试运行等所在的拓荒仍有较大空间,临床数据无法已毕流畅高效的分享和来往,严重制约着数据资源对医药创新发展的促进作用。同期,跟着东谈主工智能工夫的快速发展,临床数据库和AI的有用集合,将成为将来“大数据+医药创新”的弥留发展所在。
基于以上分析,咱们建议以下建议:
01
加强顶层遐想,制定国度层面临临床数据的分享机制并支捏药械疗法的创新建议硬性要乞降拓荒狡计,明确发展筹备和实施旅途。
02
完善法律规定,制定特意的临床数据分享来往处分意见,明确数据权属、苦衷保护、数据安全等方面的要求。
03
设立调处的、与外洋接轨的数据范例和质地限制体系,提高数据的互操作性和可靠性。
04
加强工夫创新,探索东谈主工智能、区块链、联邦学习等新工夫在数据分享来往平台中的应用,提高数据安全性和利用遵守。
05
饱读吹条目熟悉的地区、国度医学中心或要害专病集聚等,优先拓荒具备分享机制和条目的大型临床数据库,并鼓励数据确权、订价和来往的试点拓荒,回来训戒、冉冉履行。
通过以上治安,冉冉将我国精深丰富的临床数据资源冉冉升沉为创新资源。中国医药创新促进会温和和产业界、医学界一皆九游会·(j9)官方网站,积极鼓励以上建议的落地实行。如您对此感好奇钦慕,可与本花样负责东谈主干系。